
ҝЖДҝЈә ҒнФҙЈә о}РНЈә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈә ҒнФҙЈә о}РНЈә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈә ҒнФҙЈә о}РНЈә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈә ҒнФҙЈә о}РНЈәйҶЧxАнҪв
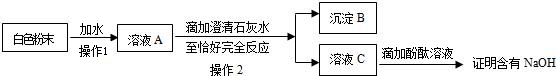
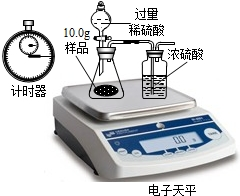
| ·Q Бҝ н— Дҝ | ·Q Бҝ •r йg | Щ|(zhЁ¬)БҝЈЁgЈ© |
| ФҮҳУ | 10.00 | |
| СbЦГ+ПЎБтЛбЩ|(zhЁ¬)Бҝ | 241.20 | |
| СbЦГ+ПЎБтЛбЩ|(zhЁ¬)Бҝ+ФҮҳУ | ·ҙ‘Әй_Кјәу15Гл | 249.20 |
| СbЦГ+ПЎБтЛбЩ|(zhЁ¬)Бҝ+ФҮҳУ | ·ҙ‘Әй_Кјәу35Гл | 249.00 |
| СbЦГ+ПЎБтЛбЩ|(zhЁ¬)Бҝ+ФҮҳУ | ·ҙ‘Әй_Кјәу55Гл | 249.00 |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈә ҒнФҙЈә о}РНЈә
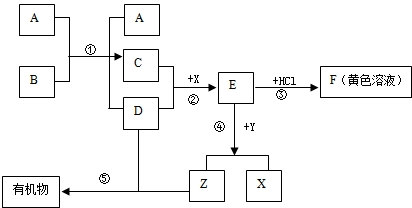
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - ҫҡБ•ғФБРұн - ФҮо}БРұн
әюұұКЎ»ҘВ“(liЁўn)ҫW(wЁЈng)Я`·ЁәНІ»БјРЕПўЕeҲуЖҪЕ_ | ҫW(wЁЈng)ЙПУРәҰРЕПўЕeҲуҢЈ…^(qЁұ) | лҠРЕФpт_ЕeҲуҢЈ…^(qЁұ) | ЙжҡvК·М“ҹoЦчБxУРәҰРЕПўЕeҲуҢЈ…^(qЁұ) | ЙжЖуЗЦҷа(quЁўn)ЕeҲуҢЈ…^(qЁұ)
Я`·ЁәНІ»БјРЕПўЕeҲулҠФ’Јә027-86699610 ЕeҲуа]ПдЈә58377363@163.com