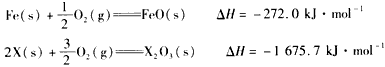���P(gu��n)��(x��)�}
0 10371 10379 10385 10389 10395 10397 10401 10407 10409 10415 10421 10425 10427 10431 10437 10439 10445 10449 10451 10455 10457 10461 10463 10465 10466 10467 10469 10470 10471 10473 10475 10479 10481 10485 10487 10491 10497 10499 10505 10509 10511 10515 10521 10527 10529 10535 10539 10541 10547 10551 10557 10565 203614
��Ŀ��
��Դ��0103 �����}
�}�ͣ��Ɣ��}
A����B�������C���� D�������E����ԭ����(sh��)�����������N������Ԫ�أ���֪��
��A��C��ͬ��Ԫ�����������AԪ�ص�ԭ�Ӱ돽�Ƕ�����Ԫ��ԭ���а돽��С������
��A��B���γɽM�ɞ�A2B��A2B2�ăɷN�����
��DԪ��ԭ�����γɵ��x����ͬ����Ԫ��ԭ���γɵ��x���а돽����С����������DԪ��ԭ�ӵ��������Ӕ�(sh��)��EԪ��ԭ���������Ӕ�(sh��)��һ�����
Ո�ش�
��1��AԪ����________��CԪ����_________�������DԪ����_________��EԪ����_________�������Ԫ�ط�̖��
��2��������A2B2���������W(xu��)�I______________���ʽ��____________��
��3��B��E�γɃɷN��Ҋ��������_________��_________������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���Ĵ�ʡ�߿����}
�}�ͣ��Ɣ��}
������Ԫ���γɵij�Ҋ�ǽ��ٹ��w���|(zh��)A�c��Ҋ���ن��|(zh��)B���ڼӟ�l���·���(y��ng)���ɻ�����C�����C�cˮ����(y��ng)���ɰ�ɫ����D�͚��wE�������D�������ڏ�(qi��ng)�������Ҳ�����ڏ�(qi��ng)�A��E�������՚���ȼ���a(ch��n)���̼��Ԛ��wG����G�ڴ�����܌�(d��o)��������γ�������E�������������c��Һ���յõ��oɫ��ҺF������ҺF�ڿ՚����L�ڷ��ðl(f��)������(y��ng)����������֮һ��H�����H�c�^�����c�ĽY(ji��)��(g��u)�ͻ��W(xu��)���|(zh��)��������������Һ�@�Sɫ����Ո�ش����І��}��
��1���M�Ɇ��|(zh��)A��Ԫ��λ�����ڱ���________���������________�塣
��2��B�c�������c��Һ����(y��ng)�Ļ��W(xu��)����ʽ�飺________________________���
��3��G�c�����c�����ԗl���·���(y��ng)�����������������������ȡ�ԓ����(y��ng)�������a(ch��n)���________�����(d��ng)����
2mol�������ȕr���D(zhu��n)�����________mol����
��4����ҺF�ڿ՚����L�ڷ�������H�Ļ��W(xu��)����ʽ�飺________________________�����
��5��H����Һ�cϡ���ᷴ��(y��ng)�ĬF(xi��n)���________________________����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ�����߿����}
�}�ͣ��Ɣ��}
X���Y����Z��L�������M��NԪ�ص�ԭ����(sh��)�������������X��Y�����Z�������L�ǽM�ɵ����|(zh��)�Ļ��A(ch��)Ԫ������M�ǵؚ��к�����ߵĽ���Ԫ�����������ش����І��}��
��1��L��Ԫ�ط�̖��________��M��Ԫ�����ڱ��е�λ�Þ�________________���������NԪ�ص�ԭ�Ӱ돽�Ĵ�С�������____________________����Ԫ�ط�̖��ʾ�������
��2��Z�����X��Ԫ�ذ�ԭ�Ӕ�(sh��)Ŀ��l��3��2��4��(g��u)�ɷ���A��B�����A�����ʽ��____________�����B�ĽY(ji��)��(g��u)ʽ��____________�����
��3������se�������w�������Ԫ�أ��cLͬһ��������Seԭ�ӱ�Lԭ�Ӷ��ɂ���ӌ�������tSe��ԭ����(sh��)��
_______������߃r�������(y��ng)��ˮ���ﻯ�W(xu��)ʽ��_______��ԓ��2 ~ 5����Ԫ�؆��|(zh��)�քe�cH2����(y��ng)����
lmol��B(t��i)�仯��ķ���(y��ng)������������ʾ����1mol�����䷴��(y��ng)�����__________������ĸ��̖�����
a��+99��7 mol��L-1 b��+29��7 mol��L-1 c����20��6 mol��L-1 d����241��8 kJ��mol-1
��4����M���|(zh��)��ꖘO���ʯī��ꎘO��NaHCO3��Һ��늽�Һ�M(j��n)��늽�����������y����R������R�ܟ�ֽ����ɻ�����Q������ꖘO����R��늘O����(y��ng)ʽ��_____________________���������R����Q�Ļ��W(xu��)����ʽ��___________________����______________________������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ��Ɣ��}
A�������B���C���������Ԫ�أ����γ�A2C��BC2�ɷN���������A��B������C��ԭ����(sh��)�����f����Aԭ�ӵ�K�ӵ���Ӕ�(sh��)Ŀֻ��һ��������Bλ��A����һ���ڣ������������Ӕ�(sh��)��K�Ӷ�2����������Cԭ�Ӻ�����������Ӕ�(sh��)�ȴ������Ӕ�(sh��)��2����
��1��������Ԫ�ط�̖�քe�飺A___________ ������B_____________ ��C________________ �������
��2��BC2����_____________ �I�M�ɵ�____________________ ����O�ԡ��ǘO�ԡ������ӡ�
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���߿����}
�}�ͣ��Ɣ��}
���������ҡ�������������ǰ������Ԫ���γɵ�������������ӿ���(sh��)������������֪�������������������pԭ�ӷ��ӻ�ؓ(f��)���r�pԭ����x�ӣ�����ԭ��������
��1�����c�}�x�ӽM�ɵ��x�ӻ������ˮ����(y��ng)�a(ch��n)��һ�N��ȼ�Ԛ��w������(y��ng)�Ļ��W(xu��)����ʽ��___________________________
��2�����ڸߜؕr��һ�N߀ԭ���������Ո�û��W(xu��)����ʽ��ʾ���ڹ��I(y��)�ϵ�һ�N��Ҫ��;��_________________
��3����һ���l������������cO2����(y��ng)�Ļ��W(xu��)����ʽ��_____________________����
��4������Ԫ�ط�̖��______________���������ԭ�ӽY(ji��)��(g��u)ʾ��D��___________________��
��5������������ľ��w�Y(ji��)��(g��u)�c____________�ľ��w�Y(ji��)��(g��u)�����������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���������΅^(q��)�߿����}
�}�ͣ��Ɣ��}
��֪X�����Y��Z���NԪ�ص�ԭ����(sh��)֮�͵���42������XԪ��ԭ�ӵ�4p܉������3��δ�Ɍ���ӣ�YԪ��ԭ�ӵ������2p܉������2��δ�Ɍ�����������X��Y���γɻ�����X2Y3��ZԪ�ؿ����γ�ؓ(f��)һ�r�x�������
Ո�ش����І��}��
��1��XԪ��ԭ�ӻ��B(t��i)�r������Ų�ʽ��____________���ԓԪ�صķ�̖��________________�����
��2��YԪ��ԭ�ӵăr����ӵ�܉����ʾʽ��_______________�������ԓԪ�ص����Q��_____________���
��3��X�cZ���γɻ�����XZ3�������ԓ������Ŀ��g��(g��u)�͞�________________�����
��4����֪������X2Y3��ϡ������Һ�пɱ������\߀ԭ��XZ3��������a(ch��n)��߀��ZnSO4��H2O�������ԓ����(y��ng)�Ļ��W(xu��)����ʽ��_________________________���
��5�����^X�Ě仯���cͬ��ڶ�������������Ԫ�����γɵĚ仯�ﷀ(w��n)���ԡ����c�ߵͲ��f������________________________________��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ʡ�߿����}
�}�ͣ��Ɣ��}
Q���R��X�������Y�������Z��NԪ�ص�ԭ����(sh��)�����f�������֪��
��Z��ԭ����(sh��)��29������ľ������������Ԫ���������
��Yԭ�Ӄr��ӣ������ӣ��Ų���msnmpn��
��Rԭ�Ӻ�̎L����Ӕ�(sh��)���攵(sh��)���
��Q��Xԭ��p܉������Ӕ�(sh��)�քe��2��4����
Ո�ش����І��}��
��1��Z2+�ĺ�������Ų�ʽ��___________������
��2����[Z(NH3)4]2+�x���У�Z2+�Ŀ�܉������NH3���������ṩ��____________�γ���λ�I���
��3��Q�cY�γɵ���Κ�B(t��i)�仯��քe��ס������������Д����_����____________�����
a����(w��n)���ԣ���>���������c����>��
b����(w��n)���ԣ���>��������c����<��
c����(w��n)���ԣ���<������������c����<��
d����(w��n)���ԣ���<�ң����c����>��
��4��Q�������R����Y���NԪ�صĵ�һ��x�ܔ�(sh��)ֵ��С���������____________����Ԫ�ط�̖ �������
��5��Q��һ�N�仯�����������|(zh��)����26�������������Ц��I�c���I���I��(sh��)֮�Ȟ�____________
��6����NԪ����������ؓ(f��)������c��С�ăɷN�ǽ���Ԫ���γɵľ��w����____________����w��ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ʡ�߿����}
�}�ͣ��Ɣ��}
W�������X�����Y�����Z�����ڱ�ǰ36̖Ԫ���е��ķN��ҊԪ���������ԭ����(sh��)��������W����Y���������nj�(d��o)���������Ҫ���|(zh��)�����X�Ļ��B(t��i)ԭ�Ӻ�����7��ԭ��܉���������������Z���γɼtɫ����u�tɫ����Z2O�ͺ�ɫ��
ZO�ɷN�����
��1��Wλ��Ԫ�����ڱ���________���ڵ�________���������W�Ě�B(t��i)�仯�ﷀ(w��n)���Ա�_______H2O(g) �����(qi��ng)��������������
��2��Y�Ļ��B(t��i)ԭ�Ӻ�������Ų�ʽ��____________�����Y�ĵ�һ��x�ܱ�X��________�����С����������
��3��Y����߃r�������(y��ng)ˮ����ĝ���Һ�cZ�Ć��|(zh��)����(y��ng)�Ļ��W(xu��)����ʽ��________________________
��4����֪���Д�(sh��)��(j��)
X�Ć��|(zh��)��FeO����(y��ng)�ğữ�W(xu��)����ʽ��________________________
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ��Ɣ��}
X��Y�������Z���W��Ԫ�����ڱ�ǰ�������е��ķN��ҊԪ�أ������P(gu��n)��Ϣ���±�
��1��Yλ��Ԫ�����ڱ���_____����_____��������Y��Z����߃r�������(y��ng)��ˮ����������^��(qi��ng)����
___________�������W(xu��)ʽ����
��2��XY2��һ�N���õ��܄����XY2�ķ����д���_______�����I��������H�DY��H�DZ�ɷN���r�I����������I�ĘO���^��(qi��ng)����_________����I�L�^�L����__________��
��3��W�Ļ��B(t��i)ԭ�Ӻ�������Ų�ʽ��______________����W2Y�ڿ՚����џ�����W2O�Ļ��W(xu��)����ʽ��
____________________����
��4��̎����XO��YO2��������Ⱦ��һ�N������������nj����ڴ����������D(zhu��n)������|(zh��)Y�������֪��
XO(g)+1/2O2(g)=XO2(g) ��H=��283��0 kJ��mol-1
Y(g)+ O2(g)=YO2(g) ��H=��296��0 kJ��mol-1
�˷���(y��ng)�ğữ�W(xu��)����ʽ��_____________________�����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ��Ɣ��}
X��Y����Z�������L�����M��NԪ�ص�ԭ����(sh��)��������������X�������Y��Z���L�ǽM�ɵ����|(zh��)�Ļ��A(ch��)Ԫ�أ�M�ǵؚ��к�����ߵĽ���Ԫ������������ش����І��}��
��1��L��Ԫ�ط�̖��________ ������M��Ԫ�����ڱ��е�λ�Þ�________________����NԪ�ص�ԭ�Ӱ돽�Ĵ�С�������____________����Ԫ�ط�̖��ʾ���������
��2��Z������X��Ԫ�ذ�ԭ�Ӕ�(sh��)Ŀ��l��3��2��4��(g��u)�ɷ���A��B����A�����ʽ��________________����B�ĽY(ji��)��(g��u)ʽ��
____________����
��3������se�������w�������Ԫ�أ��cLͬһ���������Seԭ�ӱ�Lԭ�Ӷ��ɂ���ӌ�����tSe��ԭ����(sh��)��_______�������߃r�������(y��ng)��ˮ���ﻯ�W(xu��)ʽ��________________________��ԓ��2 ~ 5����Ԫ�؆��|(zh��)�քe�cH2����(y��ng)����l mol��B(t��i)�仯��ķ���(y��ng)�������������ʾ����1 mol�����䷴��(y��ng)�����__________������ĸ��̖�������
a��+99��7 mol��L-1 b��+29��7 mol��L-1 c����20��6 mol��L-1 d����241��8 kJ��mol-1
��4����M���|(zh��)��ꖘO��ʯī��ꎘO���NaHCO3��Һ��늽�Һ�M(j��n)��늽⣬�����y����R������R�ܟ�ֽ����ɻ�����Q������ꖘO����R��늘O����(y��ng)ʽ��_____________________�������R����Q�Ļ��W(xu��)����ʽ��________________________�����
�鿴�𰸺ͽ���>>