���P(gu��n)���}
0 14136 14144 14150 14154 14160 14162 14166 14172 14174 14180 14186 14190 14192 14196 14202 14204 14210 14214 14216 14220 14222 14226 14228 14230 14231 14232 14234 14235 14236 14238 14240 14244 14246 14250 14252 14256 14262 14264 14270 14274 14276 14280 14286 14292 14294 14300 14304 14306 14312 14316 14322 14330 203614
��Ŀ��
��Դ�������߿����}
�}�ͣ�����}
�����Ј��N�۵�ij�Nʳ�þ����}���b�����������f��
(1)������c�⻯������ԗl���°l(f��)�����·���(y��ng)�����ƽ���W(xu��)����ʽ�������W(xu��)Ӌ����(sh��)���ڿհ�̎����
___KIO3��___KI��___H2SO4 =___K2SO4��___I2��___H2O
(2)��������(y��ng)���ɵ�I2�������Ȼ�̼�z������������Ȼ�̼��Һ�м���Na2SO3ϡ��Һ�������I2߀ԭ���Ի������Ȼ�̼������
��Na2SO3ϡ��Һ�cI2����(y��ng)���x�ӷ���ʽ��___________________��
��ij�W(xu��)���O(sh��)Ӌ�������Ȼ�̼�IJ������E�飺
a����������Ȼ�̼��Һ���ڷ�Һ©��������
b�������m��Na2SO3ϡ��Һ��
c�����x����Һ�w�����
�����O(sh��)Ӌ���z©�IJ������������E�е�λ����______________________�����
(3)��֪��I2��2S2O32-==2I-��S4O62-��ij�W(xu��)���y��ʳ�þ����}�ĵ⺬��������䲽�E�飺
a���ʴ_�Qȡw gʳ�}����������m�����sˮʹ����ȫ�ܽ�����
b����ϡ�����ữ������Һ��������������KI��Һ���ʹKIO3�cKI����(y��ng)��ȫ��
c���Ե�����Һ��ָʾ����������μ������|(zh��)������Ȟ�2.0��10-3 mol/L��Na2S2O3��Һ10.0 mL��ǡ�÷���(y��ng)��ȫ����
���Д�c�з���(y��ng)ǡ����ȫ����(j��)�ĬF(xi��n)����________________________��
��b���(y��ng)���a(ch��n)����I2�����|(zh��)������________mol������
�۸���(j��)���ό��Ͱ��b���f�������y�����}�ĵ⺬����(�Ժ�w�Ĵ���(sh��)ʽ��ʾ)_________mg/kg������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������}
�}�ͣ�����}
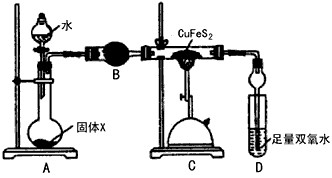
ijͬ�W(xu��)��y���S�~�V����ĺ�������Ҫ�ɷ֞�CuFeS2���s�|(zh��)�������O(sh��)Ӌ�������Qȡ0.2g�м����S�~�V��Ʒ������ߜ��º������ַ���(y��ng)��������a(ch��n)���������~���������������ij�N�F�������
Ո�ش����І��}��
(1)�b��A��ʢˮ�ăx�����Q��________�����b��B��������_______
(2)���wX�ǵ��Sɫ���|(zh��)��������ɷֿ�����_______����b��D�аl(f��)������(y��ng)�Ļ��W(xu��)����ʽ��________________
(3)����(y��ng)��C�К����Ĺ��w�ʺ�ɫ����ijͬ�W(xu��)�Ɯy���ɵ��F�������������FeO��Fe3O4�е�һ�N�����Ո�O(sh��)Ӌ�������z���ɷ�____________________
(4)����D�е���Һ�֞��ĵȷ��D(zhu��n)�����Ă��F��ƿ�������0.4 mol/L��NaOH�˜���Һ�ζ����_���K�c�r�������Ę˜���Һ��ƽ��ֵ��25. 00 mL�����tԓ�S�~�V����ĺ�����________����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��������ĩ�}
�}�ͣ�����}
ij�y����ˮ�Ļ�����ĩ�г�����̿���������߀���ܺ����F��������X�Ć��|(zh��)��������ijһ�N�������������ijУ���С�Mͬ�W(xu��)ͨ�^���_��ԓ������ĩ�ijɷ����
���E��
��ȡmg���w��ĩ��һ�������У���������NaOHϡ��Һ����К��w�a(ch��n)�����^�V�õ����wA�͟oɫ��ҺB���
�ڌ��������ù��wAϴ���ֳɃɷݡ�һ�ݼ���CuSO4��Һ�����o���@׃�������һ�ݼ�������ϡ���ᣬ�^�V �õ����wC�����Sɫ��ҺD�������
Ո�ش������}��
(1)�������аl(f��)������(y��ng)���x�ӷ���ʽ__________________
(2)���wC�c�������ܟ��l(f��)������(y��ng)�Ļ��W(xu��)����ʽ��_______________
(3)�����Sɫ��ҺD�м����F�ەr�l(f��)������(y��ng)���x�ӷ���ʽ��________________
(4)�����������ԫ@�ýY(ji��)Փ����������ĩ��һ������̿�ۺ�__________����W(xu��)ʽ��������ͬ�������FԪ�ص����|(zh��)������_________���������Ҫ�_�����FԪ�ص����|(zh��)������߀���M��һ����ԓ������___________
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ģ�M�}
�}�ͣ�����}
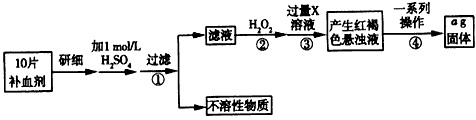
���၆�F���w(FeSO4��7H2O)���t(y��)ˎ�Ͽ����aѪ��������ij�n��С�M�y��ԓ�aѪ�����FԪ�صĺ��������E����
Ո�ش����І��}��
(1)���E�ڼ����^��H2O2��Ŀ�Ğ�____________________����
(2)���E���з���(y��ng)���x�ӷ���ʽ��_______________________�����
(3)���E���е�һϵ�в������Ξ飺�^�V�����____ ���Ɵ��������____��������Q�����
(4)���o�p�ģ��tÿƬ�aѪ�����FԪ�ص��|(zh��)����________ g(�ú�a�Ĵ���(sh��)ʽ��ʾ��������û���)�������
(5)ԓС�M��Щͬ�W(xu��)�J����KMnO4��Һ�ζ�Ҳ���M���FԪ�غ����Ĝy�������������(y��ng)ԭ��飺5Fe2++MnO4-+8H+
=5Fe3++Mn2++4H2O
�ٌ��ǰ�������Ҫ���_����һ�����|(zh��)������ȵ�KMnO4��Һ250 mL�����ƕr��Ҫ�ăx������ƽ����������������������z�^�ι��⣬߀��Ҫ�IJ����x����_________����
����������е�KMnO4��Һ��Ҫ�ữ�������������ữ������_________��
a��ϡ���� b��ϡ���� c��ϡ�}�� d��������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ģ�M�}
�}�ͣ�����}
�������c(NaClO2)��һ�N��Ҫ�ĺ������������������Ҫ����ˮ�������Լ�����Ʒ��Ư�ס��^�����䷨���a(ch��n)�������c�IJ������E���£�
�ٌ������c(NaClO3)���}����뵽ClO2�l(f��)����������
�ڌ��a(ch��n)����ClO2���w�ڷ�(w��n)���b������ˮ���պ��������ټ���NaOH���p��ˮ�����
���ڹ��w���x�b�����M�з��x�������õ��������c�����
��֪NaClO2���ܽ���S�ض����߶�����������m���l���¿ɽY(ji��)������NaClO2��3H2O����NaClO2�ډA�ԗl���·�(w��n)�����^���������ԇ�ش����І��}��
(1)��ClO2�l(f��)������ͬ�r���Ț�a(ch��n)���������t��ClO2�l(f��)�����аl(f��)������(y��ng)�Ļ��W(xu��)����ʽ��_____________��
(2)��ClO2��(w��n)���b���У�H2O2��_______ ���x����̖��������
A�������� B��߀ԭ�� C����������������߀ԭ�� D���Ȳ���������Ҳ����߀ԭ��
(3)�ڌ����ģ�M�����w���x�b�á��еļ��g(sh��)������M�еČ�������___________��������Ⱥ�����������̖�������
A���^�V B���ӟ� C�����l(f��) D����Һ E�����s F����s
(4)��(j��ng)����Y�Ͽ�֪���������pH��2.0�r�����ClO2-�ܱ�I-��ȫ߀ԭ��Cl-�����y����Ʒ��NaClO2�ĺ�����������F(xi��n)�M���� �²�����
�ٲ��E���аl(f��)������(y��ng)���x�ӷ���ʽ��______________ �������E�����_���ζ��K�c�r�ĬF(xi��n)����___________
���������ζ���������ȥ��VmL Na2S2O3��Һ������t��Ʒ��NaClO2���|(zh��)���֔�(sh��)��_____������ĸ��ʾ���������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ģ�M�}
�}�ͣ�����}
ij���������W(xu��)С�M��ͬ�W(xu��)�_չ�y��Na2CO3��NaCl�Ĺ��w�������Na2CO3�|(zh��)���֔�(sh��)��̽��������������Ќ���--���w����������
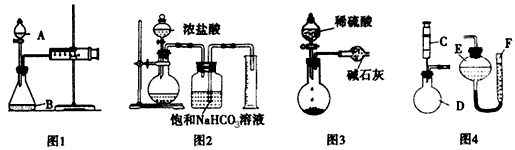
(1)��ͬ�W(xu��)�ÈD1��ʾ�b����������mg������c����ϡ���ᷴ��(y��ng)����������y���a(ch��n)����CO2���w���w�e�����������_ʼ�r�z��ԓ�b�Ú����Եķ�����_____________________�������
(2)��ͬ�W(xu��)�ÈD2��������D3�b�Üy��CO2���|(zh��)�����@�ɂ��b�þ��������@ȱ�������Ոָ���D2�п�������y���Y(ji��) ��ƫ��ă�̎�e�`____________���_____________�������Ո������D3�b�������ʹ�y���Y(ji��)������ƫ�����Ҫԭ����____________����ʹ�y���Y(ji��)������ƫС����Ҫԭ����____________������ƫ�����ƫС��ԭ�����һ�l�����
(3)��ͬ�W(xu��)ͨ�^���²��E���ÈD4�b���M�Мy�������Ո�a���ȱ�Č��E�����
�ٙz��b�õĚ����Ժ���C�м���VmLϡ������� D�м���mg��Ʒ��E�м����NaHCO3��Һ������������b���B�ӣ�
��_____________________����
��ӛ�FҺ��Ŀ̶Ȟ�a mL(�˜ʠ�r)�����
�܌�C������ע��D��ʹ���ַ���(y��ng)������
��______________________���
��ӛ�FҺ��Ŀ̶Ȟ�b mL(�˜ʠ�r������b>a)��
(4)����(j��)��ͬ�W(xu��)���õČ�(sh��)��(j��)�����Ӌ���Ʒ��Na2CO3�ĺ�����_____________�������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ģ�M�}
�}�ͣ�����}
����̽���Aʽ̼���V[mMgCO3��nMg(OH)2��xH2O]�ĽM�������ij���W(xu��)С�M�H�������Ѓx���M�bһ�������b���M�Ќ��A�փx��ʡ�ԣ��������
�ش����І��}��
(1)���r��(y��ng)���b����ͨ��՚�����������՚������������������b���B�����飨�b�ò��؏�(f��)ʹ�����������x���ӿ���ĸ��̖�����՚��( )( )��( )( )��( )( )��( )( )��(g)����
(2)�B�Ӻ��b�������z���b�Ú�������������b��ˎƷ����������ӟ�ǰ��(y��ng)�M�еIJ�����________________�������
(3)�x��B��������_________________��������x��A��������_________________����
(4)��ͬ�W(xu��)�J��(1)�е�������b����ȱ���������䲻��֮̎��___________�����M������___________�����
(5)���b�ø��M���M�Ќ��Qȡһ�����ĉAʽ̼���V��Ʒ�����ַ���(y��ng)��õ�1.6g���������1.32g������̼��0. 72 gˮ�������t�ˉAʽ̼���V�Ļ��W(xu��)ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ����x�}
ij�о��ԌW(xu��)��С�M�O(sh��)Ӌ�������y�������c��Ʒ���^�����c�ĺ�������������ۣ���ȡһ���|(zh��)���Ę�Ʒ��������У���������ϡ�}������������ʹ֮��ַ���(y��ng)���ڌ�����(y��ng)�����Һ�������l(f��)�������l(f��)�����������s���Q���������������l(f��)�^���У��ֲ��ض��^������������Һ���w�R�����t���Y(ji��)����
A��ƫ��
B��ƫ��
C���oӰ�
D���o����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������}
�}�ͣ�����}
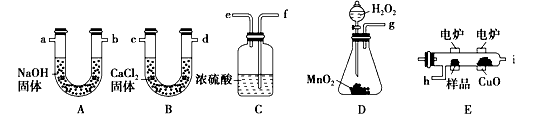
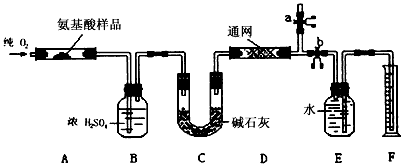
���W(xu��)�ϳ���ȼ�����_���ЙC��ĽM���������@�N��������늠t�ӟ�r�ü��������܃�(n��i)��Ʒ������(j��)�a(ch��n)���|(zh��)���_���ЙC��ĽM��������b�����D��ʾ���������ȼ�����_���ЙC�ﻯ�W(xu��)ʽ���õ��b��������
�ش����І��}��
(1)�a(ch��n)�������ⰴ����������������x���b�ø���(d��o)�ܵ��B�������____________��
(2)C�b���Н�H2SO4�����Þ�____________���
(3)D�b����MnO2������____________��
(4)E��CuO������______________����
(5)���ʴ_�Qȡ0.90 g��Ʒ(ֻ��C�����H�������O���NԪ���еăɷN�����N)��(j��ng)���ȼ���������A���|(zh��)������1.32 g��B���|(zh��)������0.54 g������tԓ�ЙC���ʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
�������ȼ�����y��ij�N������(CxHyOzNp)�ķ��ӽM�����ȡwgԓ�N��������ڼ����г��ȼ��������
CO2��H2O��N2�����F(xi��n)���D��ʾ�b���M�Ќ��F���_�����F�A��������ƾ�����δ�������������Ո�ش����P(gu��n)���}
��1������_ʼ�r��������ȴ��_ֹˮ�Aa�����P(gu��n)�]ֹˮ�Ab���ͨһ�Εr�g�ļ���������@������Ŀ����__________���֮��t���P(gu��n)�]ֹˮ�A________����������_ֹˮ�A__________��
��2�������b������Ҫ�ӟ���У����b�ô�̖��________����������r��(y��ng)���cȼ________̎�ľƾ������
��3���b��A�аl(f��)������(y��ng)�Ļ��W(xu��)����ʽ��_____________________________������
��4���b��D��������______________________________��
��5���錢N2����ˮ���w�e�y���������(y��ng)ǰ��(y��ng)���B��E��F�b�õIJ�����(d��o)���г�M________��ˮ���՚�����⣩������������________________________���
��6���xȡN2����ˮ���w�e�r��Ҫע�⣺��________________________���������________________________���
��7������Мy��N2���w�e��VmL���ѓQ��ɘ˜ʠ�r������_���˰�����ķ���ʽ����߀��õ��Ĕ�(sh��)��(j��)�У�����ĸ��________________������
A.���ɶ�����̼���w���|(zh��)��
B.����ˮ���|(zh��)��
C.ͨ��������w�e
D.ԓ�������Ħ���|(zh��)��
��8��������b����B��C���B�����׃?y��u)�C�����B����ԓ����Ŀ���ܷ��_�������������________________________________________�����
�鿴�𰸺ͽ���>>