���P���}
0 14873 14881 14887 14891 14897 14899 14903 14909 14911 14917 14923 14927 14929 14933 14939 14941 14947 14951 14953 14957 14959 14963 14965 14967 14968 14969 14971 14972 14973 14975 14977 14981 14983 14987 14989 14993 14999 15001 15007 15011 15013 15017 15023 15029 15031 15037 15041 15043 15049 15053 15059 15067 203614
��Ŀ��
��Դ������ʡ��ĩ�}
�}�ͣ����x�}
��2.4 g�V���X�Ͻ�Ͷ��100 mL 2 mol/L�������У���ַ������������������м���2 mol/L��NaOH��Һ�������ɳ����|������r��������NaOH��Һ���w�e��
A��100 mL
B��150 mL
C��200 mL
D��240 mL
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0120 �¿��}
�}�ͣ����x�}
���I(y��)���Ƃ������β������������������δ�����յ�NO��NO2���������̎�����ŷŵ��՚�������������Ⱦ���������������������������Ⱦ���׃�U�錚�����ÉAҺ(NaOH)����β���еĵ����������������ʹ֮�D���������������c����������c��ˮ����������ԭ���������Д����л�Ϛ��w�����ܱ�NaOH��Һ��ȫ���յ���
A.1 mol O2��4 mol NO2
B.1 mol NO��4molNO2
C.1 mol O2��4mol NO
D.4 mol NO��1molNO2
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0120 �¿��}
�}�ͣ����x�}
һ�������\�c�ܶȞ�1. 85g/cm3���|���֔�(sh��)��98%������w�e50 mL�ĝ�H2SO4��ַ�����������\��ȫ�ܽ⣬ͬ�r���ɘ˜ʠ�r�µĚ��w16.8 L��������������Һϡ���0.5 L���y����Һ��c(H+) =0.1mol/L�����t���ɵĚ��w��H2��SO2���w�e�Ȟ�
A��4��1
B��1��2
C��1��4
D��3��1
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���ӱ�ʡģ�M�}
�}�ͣ����x�}
�F(xi��n)��һ�N�F��������衢�X�Ļ����19.4 g����������c�����}�ᷴ���r���������ɘ˜ʠ�r�µ�H2 11.2 L�����|����ԓ������c������NaOH��Һ���������������H2���w�eҲ��11.2 L������t����|����
A��5.6 g
B��2.8 g
C��1.4 g
D���o��Ӌ��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ʡģ�M�}
�}�ͣ�Ӌ���}
ij��Ȼ�A��������ɿ�����CO2��NaOH������Įa�����M�ɡ��Qȡ��Ȼ�A��Ʒ3.32g�����������ˮ��������}������y������CO2���w�e��672 mL���˜ʠ�r������ȡ��Ȼ�A3.32g��������þƾ����ӟ�ֽ�����ȫ���a��CO2 112 mL���˜ʠ�r����ˮ0.45g����ͨ�^Ӌ��_����Ȼ�A�Ļ��Wʽ���
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0104 ģ�M�}
�}�ͣ����x�}
��1L1.0mol��L-1NaOH��Һ����0.8molCO2��������Һ��CO32-��HCO3-�����|����֮����
A��1��3
B��2��1
C��2��3
D��3��2
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0104 ģ�M�}
�}�ͣ����x�}
�ɷN���ٷ�ĩ�Ļ����12g�������Ͷ��������ϡ�������������ژ˜ʠ�r�®a��11.2 L���w���t�@�N����������
A��Zn������Al
B��Fe��Zn
C��Al����Mg
D��Mg������Cu
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0117 ģ�M�}
�}�ͣ�Ӌ���}
��F���I(y��)�LJ��ҹ��I(y��)�Ļ��A��2008���҇���䓮a����5�|���������������λ������ij�ЌW������`���С�M���ü��ڌ���?sh��)���F�S�M�����{�У����ĵVʯ�_ʼ����F�a���Ĺ�ˇ��������ȫ��ĸ����J�R���Ո��ش�����������`���С�M���dȤ�Ć��}��
��1����6.62 g�F�Vʯ��ƷͶ���m�����}���У���ַ��������^�V�������Ȼ���ڞVҺ�м��^����NaOH��Һ������ַ������������^�V���ϴ�졢�Ɵ���4.80g Fe2O3����F(xi��n)��ԓ�F�Vʯ��ԭ�ϟ��F�������a�^�����FԪ�ؓpʧ4������Ӌ��ÿ���a1.00t���F�����F96��������������Ҫ�@�N�F�Vʯ���ه�?�������λС��(sh��)��
��2��ȡij䓘ӷ�ĩ28.12g�����Oֻ��F(xi��n)e��C�����������������г�ַ���������a���Ě��wͨ�������ij���ʯ��ˮ������õ�1g��ɫ������
��Ӌ���䓘ӷ�ĩ���F��̼���|��֮���������
����ȡ���ݲ�ͬ�|����䓘ӷ�ĩ�քe�ӵ�50g�|���֔�(sh��)��ͬ��ϡH2SO4�����������ַ�����������y�õČ�(sh��)�����±���ʾ�����˜ʠ�r���������2gH2���w�e��22.4L��
Ո�������Д�(sh��)��Ӌ��ϡ������H2SO4���|���֔�(sh��)�����
�����ڌ������^�m(x��)����mg䓘ӷ�ĩ��Ӌ�㷴���Y����ʣ��Ĺ��w�|�������? (�ú�m�Ĵ���(sh��)ʽ��ʾ)
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0117 ģ�M�}
�}�ͣ�Ӌ���}
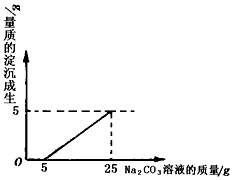
������ʯ��ʯ���s�|���c�ᷴ��������Ҳ������ˮ����ϡ�}�ᷴ����ȡ������̼��������ڜʂ䌢������ďUҺ���M�UҺ�וr�����l(f��)�F(xi��n)���������һƿδ֪�|���֔�(sh��)��Na2CO3��Һ������Q������ԓ�UҺ�������y��Na2CO3��Һ�����|���|���֔�(sh��)�������UҺ�^�V������Ȼ����UҺ�������μ�Na2CO3��Һ������Na2CO3��Һ���|���c���ɳ����|�����Pϵ��D��ʾ������
��1���ڼ���Na2CO3��Һ���^���У��_ʼ�r�]�аl(f��)�F(xi��n)�������������f���VҺ�е����|������CaCl2�����߀����______________________���
��2��Ӌ��Na2CO3��Һ�����|���|���֔�(sh��)����Ӌ��Y�����_��0.1%��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���Ϻ��߿����}
�}�ͣ�������x���}
��ʯ�ҸG�П�����ʯ�����1molCaCO3��ȫ�ֽ�����Ҫ�������������ȼ��0.453mol̼���ṩ���O�՚���O2�w�e�֔�(sh��)��0.21����N2��0.79�������tʯ�ҸG�a���Ě��w��CO2���w�e�֔�(sh��)������
A��0.43
B��0.46
C��0.49
D��0.52
�鿴�𰸺ͽ���>>