���P(gu��n)��(x��)�}
0 4115 4123 4129 4133 4139 4141 4145 4151 4153 4159 4165 4169 4171 4175 4181 4183 4189 4193 4195 4199 4201 4205 4207 4209 4210 4211 4213 4214 4215 4217 4219 4223 4225 4229 4231 4235 4241 4243 4249 4253 4255 4259 4265 4271 4273 4279 4283 4285 4291 4295 4301 4309 203614
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
������Һ��������һ���ܴ���������x�ӽM��
- A.
�o(w��)ɫ��Һ�У�Na+���MnO4-������SO42-��K+
- B.
���д���Fe3+����Һ�У�Al3+������Cu2+��Cl-�����SO42-
- C.
����Al�ܷų�H2����Һ�У�K+�����NH4+��NO3-�������Cl-
- D.
ʹ�{(l��n)ɫʯ��ԇ��׃�t����Һ�У�K+�������S2-��NO3-������OH-
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
���Ȼ���ĽY(ji��)��(g��u)�c���Ȼ�̼�(l��i)�ƣ���(du��)�����|(zh��)���Ɣ����_���ǣ��������
�����Ȼ��辧�w�Ƿ��Ӿ��w����ͨ����r��Һ�B(t��i)
�����c(di��n)�������Ȼ�̼�� �܌��������w�ķ��Ә�(g��u)��
- A.
��
- B.
�٢�
- C.
�ڢۢ�
- D.
�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�P(gu��n)���\�~��ϡ����ԭ늳صĔ�������e(cu��)�`����
- A.
�\�����O�����|(zh��)����u�pС
- B.
������\Ƭ��(j��ng)��(d��o)��(xi��n)�����~Ƭ
- C.
��ӏ��\Ƭ��(j��ng)��(d��o)��(xi��n)�����~Ƭ
- D.
���x�����~���汻߀ԭ�������a(ch��n)������
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�����f(shu��)�����_���� (����)
�ٻ�����g����ײһ���ܰl(f��)�����W(xu��)����(y��ng)
����ͨ�����Еr(sh��)Ҳ�ܰl(f��)����Ч��ײ
�����ߜضȕ�(hu��)�ӿ췴��(y��ng)���������ԭ���������˻���ӵ���Ч��ײ�Δ�(sh��)
������(y��ng)���ȕ�(hu��)�ӿ췴��(y��ng)���ʵ�ԭ���dž�λ�w�e��(n��i)��Ч��ײ�ĴΔ�(sh��)����
��ʹ�ô�������߷���(y��ng)�������ԭ��������˷��ӵ�����������ʹ��Ч��ײ�l������
���W(xu��)����(y��ng)��(sh��)�|(zh��)�ǻ�����к��mȡ��r(sh��)����Ч��ײ
- A.
�ۢܢ�
- B.
�٢ڢݡ�
- C.
�ۢܢݢޡ�
- D.
�ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�D��һ�N����������?j��)?ch��)��ϵ�y(t��ng)ԭ��ʾ��D�������f(shu��)�����_����
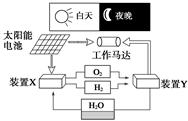
- A.
ԓϵ�y(t��ng)��ֻ����3�N��ʽ�������D(zhu��n)��
- B.
�b��Y��ؓ(f��)�O��늘O����(y��ng)ʽ��O2+2H2O+4e-===4OH-
- C.
�b��X�܌�(sh��)�F(xi��n)ȼ��늳ص�ȼ�Ϻ�����������
- D.
�b��X����Y�γɵ���ϵ�y(t��ng)�܌�(sh��)�F(xi��n)���|(zh��)�����ŷ��������܌�(sh��)�F(xi��n)���W(xu��)���c����g����ȫ�D(zhu��n)��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�����f(shu��)�����_����
- A.
���҂����õ�Ԫ�����ڱ��У�Ԫ�ر����֞���(l��i)������Ԫ�غͷǽ���Ԫ��
- B.
��Ԫ�����ڱ������ÿ��(g��)�v�еăr(ji��)��ӌӵ���ӿ���(sh��)һ�����
- C.
��Ԫ�����ڱ������Ԫ�����ڵ�����(sh��)����ԭ�Ӻ�����Ӕ�(sh��)
- D.
��Ԫ�����ڱ���������s�^(q��)��d�^(q��)��ds�^(q��)��Ԫ�ض��ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�����f(shu��)����
��ͬ�NԪ�ص�ԭ�Ә�(g��u)�ɵ������|(zh��)��ͬ����
�ڡ����������ˮ��֮����������ˮ���������f(shu��)����ͬ�|(zh��)����ˮ�ͱ����ˮ�������ߣ�
�����l(f��)�l(f��)���ķ���(y��ng)�������һ����H��0�����S��0��
�ܜy(c��)��NaA��NaB��Һ��PH���������ܱ��^HA��HB�����ԏ�(qi��ng)����
��ʳ�}���۱���ѩ�������������ʳ�}����ѩ������(hu��)��(du��)�h(hu��n)�����������L(zh��ng)���Σ������
���z�w�c��Һ�ɷN��ɢϵ���|(zh��)�^(q��)�e���z�w���ж��_(d��)���F(xi��n)�����������Һ�](m��i)������
�������_����
- A.
�ڢۢ�
- B.
�ڢ�
- C.
�ۢܢ�
- D.
�٢ݢ�
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�����x�ӷ���ʽ��(sh��)��(xi��)���_����
- A.
ϡ�����Ba(OH)2��Һ����(y��ng)��Ba2++OH-+H++SO===BaSO4��+H2O
- B.
�^(gu��)����SO2ͨ��NaOH��Һ�У�SO2+2OH-===SO+H2O
- C.
�~�ڼӟ�l�����c�����ᷴ��(y��ng)��Cu+SO+4H+===Cu2++SO2��+2H2O
- D.
SO2ʹ��ˮ��ɫ��SO2+Br2+2H2O===SO+2Br-+4H+
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�£�N2H4������������ԭ�Ӿ��_(d��)��ϡ�К��wԭ�ӵķ�(w��n)���Y(ji��)��(g��u)������ķ��c(di��n)���_(d��)113�������ȼ�����642 kJ��mol-1�����c���⼰���������Һ߀�ɘ�(g��u)��ȼ��늳�������֪�µ����ģ����D��ʾ��������������P(gu��n)�f(shu��)�����_����
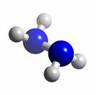
- A.
�����ɘO���I�ͷǘO���I��(g��u)�ɵķǘO�Է���
- B.
�·��c(di��n)���_(d��)l13�棬���Ɯy(c��)�·����g���γɚ��I
- C.
��ȼ���ğữ�W(xu��)����ʽ�飺N2H4��g��+ O2��g�� = N2��g�� +2H2O��g�����������H = -642 kJ��mol-1
- D.
��-����ȼ��늳�����ؓ(f��)�O��늘O����(y��ng)�飺O2 +2H2O+4e-=4OH-
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
�P(gu��n)��Na2CO3��NaHCO3�ɷN��ɫ���w�����|(zh��)���^��������Д������_����
- A.
���w��B(t��i)������Na2CO3��NaHCO3��(w��n)��
- B.
Na2CO3��NaHCO3���y����ˮ
- C.
���ƃ��ߵ����|(zh��)������ȵ���Һ�����Na2CO3��NaHCO3�ĉA�ԏ�(qi��ng)
- D.
����ߵ����|(zh��)������ȵ���Һ�м��������ϡ�}�ᣬNa2CO3��NaHCO3����(y��ng)��
�鿴�𰸺ͽ���>>


