
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
 CO
CO CO2
CO2 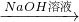 Na2CO3
Na2CO3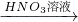 Cu��NO3��2��Һ
Cu��NO3��2��Һ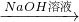 Cu��OH��2
Cu��OH��2 Fe2O3��
Fe2O3��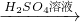 Fe2��SO4��3��Һ
Fe2��SO4��3��Һ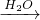 ��Ca��OH��2��Һ
��Ca��OH��2��Һ 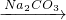 NaOH��Һ
NaOH��Һ�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ����x�}
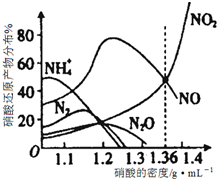 �D�Ǹ��N��ͬ�ܶȵ������c�F�����r����ͬ�ضȣ���Ҫ߀ԭ�a��ķֲ��D�����Д��������_����
�D�Ǹ��N��ͬ�ܶȵ������c�F�����r����ͬ�ضȣ���Ҫ߀ԭ�a��ķֲ��D�����Д��������_�����鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com