
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚΫβ¥πν}
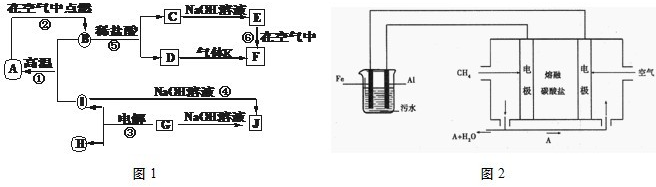
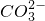 -8e-=5CO2+2H2O
-8e-=5CO2+2H2O≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚΫβ¥πν}
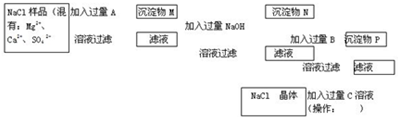
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
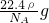
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚÜΈΏxν}
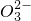 +H3O+?HC
+H3O+?HC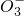 +H2O
+H2O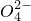 =BaSO4Γΐ+H2O
=BaSO4Γΐ+H2O≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ(l®Δi)‘¥ΘΚ ν}–ΆΘΚΫβ¥πν}
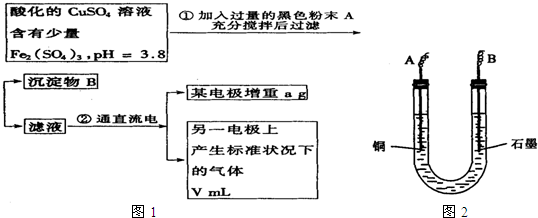
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΨöΝï(x®Σ)É‘(c®®)Ν–±μ - ‘΅ν}Ν–±μ
Κΰ±± ΓΜΞ¬™(li®Δn)ΨW(w®Θng)Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσ(b®Λo)ΤΫ≈_(t®Δi) | ΨW(w®Θng)…œ”–ΚΠ–≈œΔ≈eàσ(b®Λo)¨Θ(zhu®Γn)Ö^(q®±) | κä–≈‘pρ_≈eàσ(b®Λo)¨Θ(zhu®Γn)Ö^(q®±) | …φöv ΖΧ™üo(w®≤)÷ςΝx”–ΚΠ–≈œΔ≈eàσ(b®Λo)¨Θ(zhu®Γn)Ö^(q®±) | …φΤσ«÷ôύ(qu®Δn)≈eàσ(b®Λo)¨Θ(zhu®Γn)Ö^(q®±)
Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσ(b®Λo)κä‘£ΘΚ027-86699610 ≈eàσ(b®Λo)ύ]œδΘΚ58377363@163.com