
ν}ΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
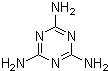 ΫϋΤΎ”–É…Φΰ ¬“ΐΤπΝΥ»Υ²ÉΒΡ‰O¥σξPΉΔΘ°
ΫϋΤΎ”–É…Φΰ ¬“ΐΤπΝΥ»Υ²ÉΒΡ‰O¥σξPΉΔΘ° NH2NH3+Θ®N2H5+Θ©+OH-
NH2NH3+Θ®N2H5+Θ©+OH- NH2NH3+Θ®N2H5+Θ©+OH-
NH2NH3+Θ®N2H5+Θ©+OH-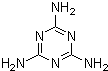 ΫϋΤΎ”–É…Φΰ ¬“ΐΤπΝΥ»Υ²ÉΒΡ‰O¥σξPΉΔΘ°
ΫϋΤΎ”–É…Φΰ ¬“ΐΤπΝΥ»Υ²ÉΒΡ‰O¥σξPΉΔΘ°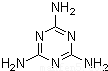
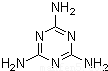
ΑΌΕ»÷¬–≈ - ΨöΝïÉ‘Ν–±μ - ‘΅ν}Ν–±μ
Κΰ±± ΓΜΞ¬™(li®Δn)ΨWΏ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσΤΫ≈_ | ΨW…œ”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | κä–≈‘pρ_≈eàσ¨ΘÖ^(q®±) | …φöv ΖΧ™üo÷ςΝx”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | …φΤσ«÷ôύ≈eàσ¨ΘÖ^(q®±)
Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσκä‘£ΘΚ027-86699610 ≈eàσύ]œδΘΚ58377363@163.com