
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΆ§≤Ϋν} ν}–ΆΘΚ≤ΜΕ®μ½Ώx™ών}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΆ§≤Ϋν} ν}–ΆΘΚ”΄Υψν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΆ§≤Ϋν} ν}–ΆΘΚ≤ΜΕ®μ½Ώx™ών}

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΆ§≤Ϋν} ν}–ΆΘΚ≤ΜΕ®μ½Ώx™ών}
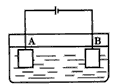
AΘ°6ΘΚ1
BΘ°4:1
CΘ°3ΘΚ1
DΘ°»Έ“β±»
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΆ§≤Ϋν} ν}–ΆΘΚ≤ΜΕ®μ½Ώx™ών}
A.4ΓΝ10-3 mol/L
B.2ΓΝ10-3 mol/L
C.1ΓΝ10-3 mol/L
D.1ΓΝ10-7mol/L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚ0115 ïΰΩΦν} ν}–ΆΘΚΧνΩ’ν}

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΫ≠ΧKΗΏΩΦ’φν} ν}–ΆΘΚ”΄Υψν}
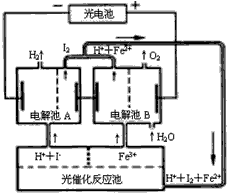
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚΗΘΫ® ΓΗΏΩΦ’φν} ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚ¨Θμ½ν} ν}–ΆΘΚÜΈΏxν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ¹μ‘¥ΘΚ±±Ψ©ΤΎ÷–ν} ν}–ΆΘΚΧνΩ’ν}
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΨöΝï(x®Σ)É‘Ν–±μ - ‘΅ν}Ν–±μ
Κΰ±± ΓΜΞ¬™(li®Δn)ΨW(w®Θng)Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσΤΫ≈_ | ΨW(w®Θng)…œ”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | κä–≈‘pρ_≈eàσ¨ΘÖ^(q®±) | …φöv ΖΧ™üo÷ςΝx”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | …φΤσ«÷ôύ(qu®Δn)≈eàσ¨ΘÖ^(q®±)
Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσκä‘£ΘΚ027-86699610 ≈eàσύ]œδΘΚ58377363@163.com