
��Ŀ�� ��Դ�� �}�ͣ�
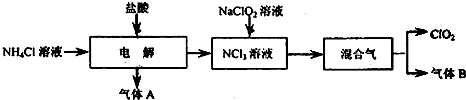
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
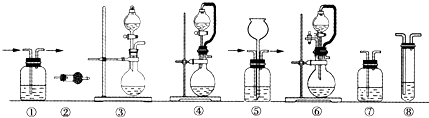
| �M�� | �Ƃ��b�� | �����b�� | �z��b��/ԇ�� | β��̎���b�� |
| A | �� | �� | ��/e | �� |
| B | �� | �� | ��/e | �� |
| C | �� | �� | ��/e | �� |
| D | �� | �� | ��/e | �� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
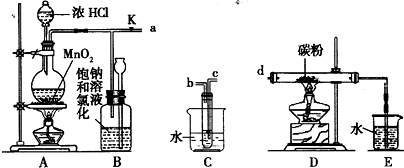
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ���x����


| ���W(xu��)ʽ | Ca��OH��2 | CaSO4 | BaCO3 | BaSO4 | MgCO3 | Mg��OH��2 |
| Ksp | 1.0��10һ4 | 7.1��10һ5 | 8.1��10һ9 | 1.08��10һ10 | 3.5��10һ5 | 1.6��10һ11 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
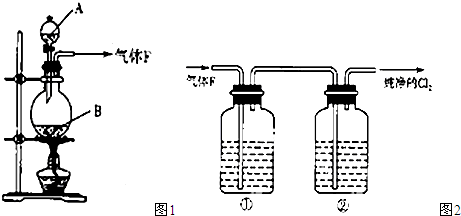
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
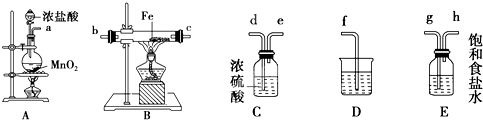
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
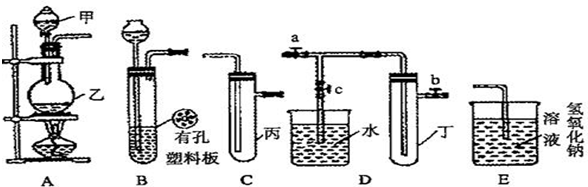
| �����̖ | ������ | �F(xi��n)�� | �Y(ji��)Փ |
| �� | ����ˮ����Ʒ�t��Һ | ��Һ��ɫ | �Ț��cˮ����(y��ng)�Įa(ch��n)����Ư���� |
| �� | ��ˮ�м���NaHCO3��ĩ | �Пoɫ���ݮa(ch��n)�� | �Ț��cˮ����(y��ng)�Įa(ch��n)������^��(qi��ng)������ |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com