
��Ŀ�� ��Դ�� �}�ͣ��Ɣ��}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
| �ض�/�� | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl�ܽ�� | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl�ܽ�� | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
| ���W(xu��)��̖ | ��1��2N2 | 3H | ��3��NO3- | �����~���~Ԫ�ػ��σr |
| ��̖�����x | 2�������� | ��2��3����ԭ�� | ������x�� | ��4��$\stackrel{+2}{Cu}$O |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� |  �����(y��n)�M | B�� |  ȡ��ˎƷ | C�� |  �Qȡ�Ȼ��c �Qȡ�Ȼ��c | D�� |  ϡጝ����� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�Ӌ���}
| ��һ�� | �ڶ��� | ������ | ���Ĵ� | |
| ����ϡ�}���|(zh��)����g�� | 10 | 10 | 10 | 10 |
| ʣ����w���|(zh��)����g�� | 9.10 | 8.45 | 7.80 | 7.80 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ���(sh��)�(y��n)̽���}
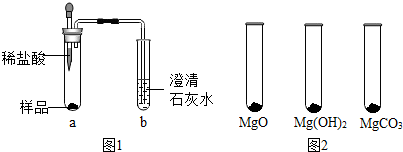
| MgO | Mg��OH��2 | MgCO3 | |
| ����ϡ�}����w�e/mL | 10.4 | 7.2 | 5.0 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ���(sh��)�(y��n)̽���}

�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com